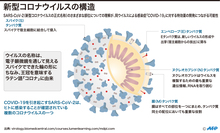
中国、ワクチン混合接種の臨床試験を初承認
このニュースをシェア
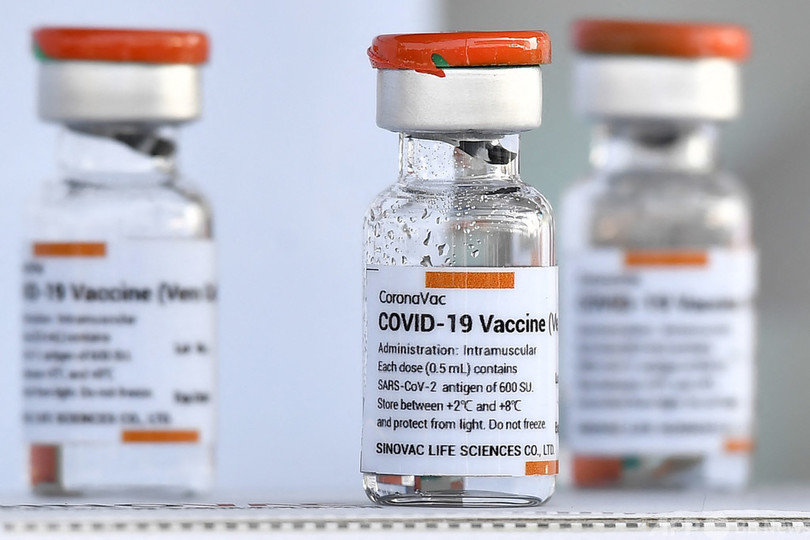
【8月11日 AFP】中国の薬事規制当局が、同国初となる新型コロナウイルスワクチンの混合接種の臨床試験を承認した。関係企業が10日、発表した。同国では変異株「デルタ株」の感染が急拡大しており、国産ワクチンの有効性を疑問視する声が出ている。
今回発表したのは、米製薬会社イノビオ・ファーマシューティカルズ(Inovio Pharmaceuticals)と中国国内の臨床試験で提携する、艾棣維欣生物製薬(Advaccine Biopharmaceuticals)。
これによると、試験では中国製薬大手シノバック・バイオテック(Sinovac Biotech)製の不活化ワクチンと、イノビオ製のDNAワクチンを組み合わせ、その有効性を調べる。
艾棣維欣の代表は、臨床前研究により「2種の異なるワクチンを接種すると、より強く、よりバランスの良い免疫応答が得られる」ことが分かったとしている。
新型コロナウイルスワクチンには、従来の不活化ワクチンや弱毒化ワクチンに加え、最先端の遺伝子技術を用いたRNAワクチンやDNAワクチンなど、幾つかの種類がある。
中国で承認されている7種のワクチンのうち5種は、2回接種を必要とする不活化ワクチンだ。
世界保健機関(WHO)はワクチン混合接種について、その安全性や免疫を強める効果の有無について判断する十分なデータがないと指摘している。
イノビオは複数の国で自社ワクチンの臨床試験を行っているが、これまで有効性に関するデータを一切発表していない。イノビオのワクチンは、中国で初めて臨床試験が実施されるDNAワクチンとなる。
中国は現在、ここ数か月で最も深刻な新型ウイルスの感染拡大に苦慮している。当局によると、感染者の多くはワクチン接種を済ませているという。(c)AFP