米FDA、コロナ抗体薬の緊急使用を許可 イーライリリー開発
このニュースをシェア
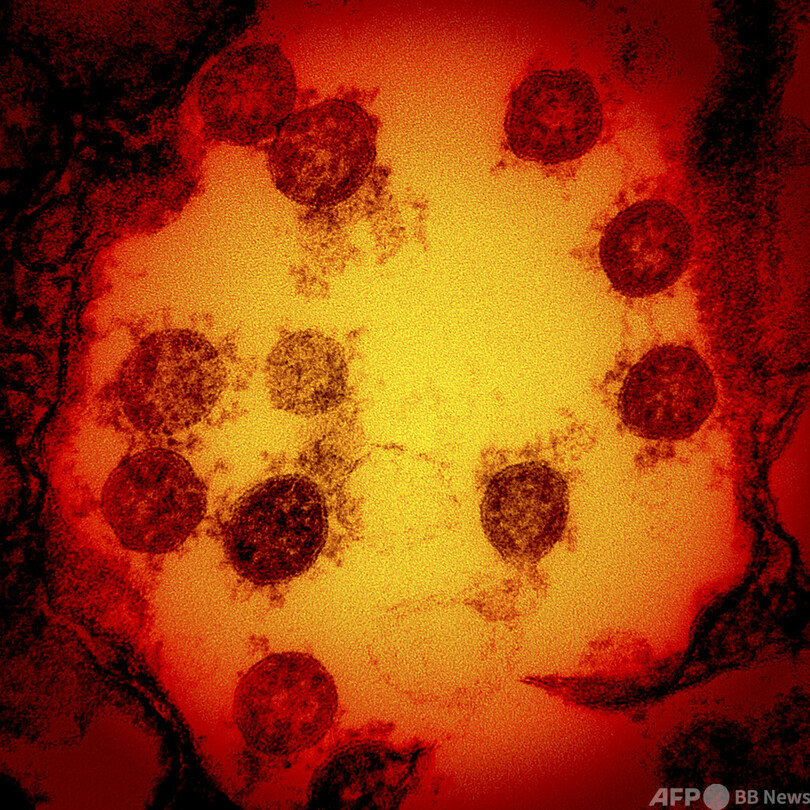
【11月10日 AFP】米食品医薬品局(FDA)は9日、米製薬大手イーライリリー(Eli Lilly)が開発した、新型コロナウイルスの人工抗体医薬品の緊急使用を許可した。入院や救急医療の受診のリスクを低下させることが証明されたという。
緊急使用が許可されたのは、「バムラニビマブ(Bamlanivimab)」。12歳以上の軽度から中程度の症状の患者で重症化リスクが高い場合に、700ミリグラムの投与が可能になる。
FDAによると、重症化リスクが高い患者を対象とした臨床試験(治験)で、実際に入院や救急医療の受診が必要となった例は、プラセボ(偽薬)を投与された患者で10%だったのに対し、バムラニビマブを投与された患者では3%にとどまったという。
ただし、重症化して免疫反応が暴走し、臓器が損傷を受けている患者への効果は示されていないため、入院患者への使用は許可されない。
バムラニビマブは、モノクローナル抗体と呼ばれる比較的新しい医薬品。モノクローナル抗体は、がんや自己免疫疾患の治療でよく知られている。(c)AFP








